GIẢI NGHĨA 30 TỪ VIẾT TẮT PHỔ BIẾN TRONG THẨM ĐỊNH DƯỢC
Thẩm định là yếu tố không thể thiếu trong ngành dược phẩm, quá trình thẩm định đòi hỏi tuân thủ cặn kẽ các quy tắc và bám sát các khái niệm, quy định chuẩn mực. Dưới đây là 30 kí tự và khái niệm cơ bản thường được nhắc tới khi thẩm định dược phẩm.

|
1. DQ: Thẩm định thiết kế (Design Qualification) |
|
2. IQ: Thẩm định lắp đặt (Installation Qualification) |
|
3. OQ: Thẩm định vận hành (Operational Qualification) |
|
4. PQ (or P1Q): Thẩm định hiệu năng (Performance Qualification) |
|
5. PV (or P2Q): Thẩm định quá trình (Process Qualification) |
|
6. URS: Đặc tả yêu cầu người dùng (User Requirement Specification) |
|
7. FAT: Nghiệm thu sản phẩm tại nhà máy sản xuất (Factory Acceptance Testing) |
|
8. SAT: Nghiệm thu sản phẩm tại nơi lắp máy (Site Acceptance Tests) |
| 9. cGMP: Thực hành sản xuất tốt theo FDA (Current - Good Manufacturing Practice) |
|
10. EU-GMP: Thực hành sản xuất tốt theo tiêu chuẩn châu Âu (European Union - Good Manufacturing Practices). |
| 11. WHO-GMP: Thực hành sản xuất tốt theo tiêu chuẩn của Tổ chức Y Tế thế giới (World Health Organization - Good Manufacturing Practices). |
|
12. PIC/S-GMP: Công ước về Thanh tra Dược và Chương trình Hợp tác Thanh tra (Pharmaceutical Inspection Co-operation Scheme). |
|
13. GSP là từ viết tắt của Good Storage Practices, nghĩa là: Thực hành tốt bảo quản thuốc. |
| 14. GDP là từ viết tắt của Good Distribution Practices – Thực hành tốt phân phối thuốc. |
| 15. GPP là từ viết tắt của Good Pharmacy Practices có nghĩa là “Thực hành tốt quản lý nhà thuốc”. |
| 16. GLP là từ viết tắt của Good Laboratory Practice, nghĩa là Hệ thống an toàn chất lượng phòng thí nghiệm. |
|
17. CFR: Quy định liên bang (Code of Federal Regulations). |
|
18. ISPE: là Hiệp hội Kỹ thuật Dược phẩm Quốc tế (The International Society for Pharmaceutical Engineering). |
|
19. GAMP: Thực hành tốt sản xuất tự động (Good Automatic Manufacturing Practice). |
| 20. GAMP® 5: Đây là khái niệm được nhắc đến trong tài liệu hướng dẫn có tên:” Phương pháp tiếp cận dựa trên rủi ro đối với đối với các hệ thống máy tính tuân thủ GxP. Tài liệu này được xuất bản bởi Hiệp hội kỹ thuật dược phẩm quốc tế ISPE. |
|
21. FDA: Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (U.S. Food and Drug Administration). |
|
22. CSV: Thẩm định Hệ thống Máy tính (Computer Systerm Validation). |
| 23. SCADA: Điều khiển giám sát và thu thập dữ liệu (Supervisory control and data acquisition). |
|
24. "R.A" đặc trưng cho độ nhám bề mặt (μm) (Arithmetical mean roughness value), là sai lệch trung bình số học được xác định bằng tất cả các điểm cao nhất và các điểm thấp nhất trong phạm vi chiều dài chuẩn L. |
|
25. "R.Z" là viết tắt của Mean roughness depth. Là chiều cao nhấp nhô trung bình cộng của 5 khoảng cách từ điểm cao nhất đến đáy thấp nhất trên bề mặt chi tiết trong phạm vi chiều dài chuẩn L. |
|
26. CE: là viết tắt của European Conformity hay CE marking, là tiêu chuẩn phù hợp với quy tắc và kỹ thuật ở các nước công nghiệp tiên tiến và các nước khác trong khối. Các sản phẩm có chứng nhận CE tức là nó đã tuân thủ đúng luật pháp của liên minh châu Âu EU và được tự do buôn bán trên thị trường các nước này. |
|
27. ATEX: Là tên chứng chỉ chống cháy nổ, được tham chiếu theo Chỉ thị 2014/34/EC của châu Âu về hệ thống chống cháy nổ trên thiết bị điện và cơ khí, linh kiện và hệ thống. |
|
28. PED: Pressure Equipment Directive, chỉ thị về thiết bị áp lực. |
|
29. VMP: Kế hoạch thẩm định gốc (Validation Master Plan). |
| 30. HVAC system qualification protocol: đề cương thẩm định hệ thống sưởi ấm, thông gió và điều hoà không khí (Heating, Ventilating and Air Conditioning system qualification). |
XEM THÊM

Bao bì vỉ (blister) đóng vai trò quan trọng trong việc bảo vệ dược chất khỏi ẩm, oxy và ánh sáng, đảm bảo chất lượng sản phẩm suốt vòng đời.

Trong ngành dược, thiết bị không chỉ cần hiện đại mà còn phải được “thẩm định” nghiêm ngặt để đảm bảo an toàn, hiệu quả và tuân thủ GMP.

Trong ngành dược phẩm, đầu tư máy móc thiết bị không chỉ là câu chuyện về chi phí mà còn liên quan đến chất lượng, tuân thủ GMP và tối ưu hóa sản xuất. Vì vậy, DQ - Design Qualification (Thẩm định thiết kế) là bước bắt buộc giúp đảm bảo thiết bị đáp ứng đúng yêu cầu ngay từ đầu!

Trong ngành dược phẩm, việc lựa chọn máy móc thiết bị không chỉ dừng lại ở yếu tố giá cả hay công nghệ, mà còn phải đáp ứng các tiêu chuẩn chất lượng nghiêm ngặt. Vì vậy, URS (User Requirement Specification) – Tài Liệu Yêu Cầu Người Dùng – đóng vai trò vô cùng quan trọng!

Việc chọn máy móc thiết bị sản xuất dược phẩm đúng cách là một trong những yếu tố quan trọng quyết định sự thành công của dự án đầu tư. Tuy nhiên, không phải ai cũng hiểu rõ và thực hiện đúng. Dưới đây là một số hướng dẫn giúp chọn máy móc thiết bị sản xuất dược phẩm đúng cách.

Việc chọn nhà cung cấp không uy tín có thể khiến doanh nghiệp đối mặt với những rủi ro nghiêm trọng

Chất lượng và độ tin cậy của thiết bị
Đảm bảo máy móc đạt tiêu chuẩn và được chứng nhận quốc tế như CE, Atex; máy phù hợp GMP và vận hành ổn định, bền bỉ. Hệ thống quản lý chất lượng theo ISO 9001.

Trong sản xuất dược phẩm hiện đại, công nghệ phun tiếp tuyến trên máy Sấy Tạo Hạt Tầng sôi đã mang lại bước đột phá. Phương pháp tiên tiến này liên quan đến việc phun chất lỏng (dung dịch hoặc huyền phù) ở góc tiếp tuyến với các hạt bột hoặc cốm đang sôi. Kết quả? Một chuyển động xoáy đảm bảo lớp tạo hạt hoặc bao chính xác, đồng đều trong thời gian rất ngắn.

Vách ngăn từ trần xuống mặt sàn, giúp người vận hành có thể nhìn thấy toàn bộ dây chuyền từ mặt trước mà không thấy ống gió.

Đảm bảo an toàn vận hành trong ngành sản xuất dược phẩm là rất quan trọng để duy trì chất lượng sản phẩm, bảo vệ con người, bảo vệ môi trường và tuân thủ các luật định. Dưới đây là một số yêu cầu chính để đảm bảo an toàn vận hành các máy bào chế trong sản xuất dược phẩm:
Chọn máy móc thiết bị sản xuất dược là quyết định quan trọng đòi hỏi sự cân nhắc cẩn thận để đảm bảo tuân thủ các yêu cầu quy định, chất lượng sản phẩm và hiệu suất vận hành.

Trong bối cảnh ngành sản xuất dược phẩm đang không ngừng thay đổi, độ chính xác và hiệu suất trở thành yếu tố quan trọng. Hệ thống Bao Viên Tự Động của TTP cách mạng hóa quy trình phủ bao bì, đảm bảo chất lượng sản phẩm tối ưu và tối giản hoá hoạt động. Hãy cùng khám phá những tính năng quan trọng làm nên sự khác biệt:

Tiến Tuấn hân hạnh giới thiệu cải tiến mới nhất của chúng tôi trong công nghệ ngăn chặn dược phẩm – Hệ thống cách ly chia liều.

Một số thách thức và lợi ích điển hình của đóng gói thuốc điều trị ung thư dưới dạng vỉ

Việc lựa chọn thiết bị sản xuất dược phẩm là một quá trình quan trọng đòi hỏi sự cân nhắc cẩn thận đối với nhiều yếu tố để đảm bảo sản xuất dược phẩm chất lượng cao và an toàn.

Bao bì dạng vỉ ngăn trẻ em được thiết kế để ngăn trẻ nhỏ có thể tò mò khám phá môi trường xung quanh và có khả năng nuốt phải các chất có hại như thuốc, nhưng vẫn cho phép người lớn mở tương đối dễ dàng.

FAT với GMP: MẮT XÍCH QUAN TRỌNG TRONG DỰ ÁN ĐẦU TƯ PHÁT TRIỂN NHÀ MÁY DƯỢC PHẨM


Quy trình tạo hạt ướt theo hai bước riêng biệt là công nghệ được sử dụng nhiều nhất và nó phù hợp với các thiết bị pha chế thuốc truyền thống như Máy trộn và tạo hạt (Mixer & Granulator) và Máy sấy và tạo hạt tầng sôi (Fluid-bed Dryer & Granulator).

Quy trình tạo hạt một bước giúp tạo hạt trực tiếp, bằng cách tạo hạt axit và hạt kiềm cùng với nhau. Thông thường, nước được sử dụng làm dung dịch tạo hạt, do đó phải kiểm soát phản ứng sủi bọt trong quá trình tạo hạt. Ethanol hoặc propanol cũng có thể được sử dụng làm dung dịch tạo hạt, tuy nhiên khi đó cần phải sử dụng thêm chất kết dính để đạt được độ kết tụ cần thiết. Có 2 dạng thiết bị được dùng để bào chế thuốc sủi theo công nghệ này

Thuốc viên sủi có ưu điểm chính là dễ sử dụng, đặc biệt hiệu quả đối với bênh nhân là trẻ nhỏ. Tuy nhiên, việc sản xuất chúng lại phức tạp hơn so với thuốc viên truyền thống, đặc biệt là việc chọn lựa công nghệ và thiết bị sản xuất.
Những ảnh hưởng của biến chủng mới thật khó có thể công bố một cách chính xác bởi khác với những chủng trước, Omicron tấn công chủ yếu vào những người trẻ và có sức để kháng tốt hơn.

Lễ ký kết hợp tác cung cấp dây chuyền ép vỉ đóng gói hoàn toàn tự động theo tiêu chuẩn GMP-EU cho US PHARMA

Đại dịch Covid-19 đã đặt ra nhiều thách thức mới cho các công ty startup dược phẩm. Cần làm gì để có thể tồn tại và phát triển nhất là trong giai đoạn này. Tờ báo StartUs Insight đã dựa trên nghiên cứu phân tích của “1745 startups tên tuổi ngành dược năm 2020”, tìm ra những startups nổi bật nhất. Để có thể biến thách thức thành cơ hội, những công ty dược phẩm đã có “bí kíp” startup sống sót qua đại dịch.


Kiểm tra chày cối và những thành phần của máy dập viên bị hao mòn hoặc bị lỗi là một trong những bước rất quan trọng để cải thiện chất lượng của thuốc viên. Có một số điểm kiểm tra mà chúng ta dễ bỏ qua nhưng có thể gây ra các vấn đề về chất lượng viên thuốc đáng kể và làm giảm tuổi thọ của chày cối. Vì vậy hãy dành một ít thời gian để kiểm tra những điểm sau để xác định độ mài mòn hoặc khiếm khuyết của chúng từ đó mau chóng cải thiện chất lượng viên thuốc và giảm chi phí chày cối

Nếu quan tâm đến việc làm đẹp thì hẳn bạn đã ít nhiều nghe đến collagen dưỡng da. Thậm chí nhiều công ty sản xuất mỹ phẩm còn cho ra những sản phẩm bôi ngoài da như kem dưỡng, lotion, serum có chứa collagen…

Ở một số nơi, khi số ca mắc #COVID-19 giảm xuống, một số biện pháp phòng chống dịch đang được gỡ bỏ...

Ngành công nghiệp dược phẩm tuân theo các yêu cầu khắt khe nhất đối với quá trình sản xuất và thiết bị được sử dụng phải tuân thủ thực hành sản xuất tốt (GMP). Khi xu hướng phát triển thuốc thay đổi, các quy trình sản xuất cũng phải thay đổi, phần lớn trong số đó hiện có thể được tự động hóa...

Cuộc khủng hoảng y tế COVID-19 mang lại những tác động và tiến bộ khoa học mạnh mẽ đồng thời cũng rút ra được những bài học kinh nghiệm quý báu cho các doanh nghiệp, tổ chức và các quốc gia trên thế giới:
Tại Trung tâm chống dộc Bệnh viện Bạch Mai đã tiếp nhận rất nhiều trường hợp bị ngộ độc do lạm dụng thuốc hạ sốt paracetamol để chữa COVID-19. Do đó, người dân nên cẩn trọng trước các bài thuốc lan truyền không rõ nguồn gốc trên mạng xã hội, trước khi sử dụng bất kỳ loại thuốc nào cần xin ý kiến bác sĩ, không được tự ý sử dụng.

Từ ngày 1/8/2021 doanh nghiệp có thể tra cứu trạng thái chứng nhận xuất xứ mẫu D trên internet. Đồng thời các doanh nghiệp nhập khẩu các lô hàng thuốc, nguyên liệu làm thuốc nhập khẩu luồng đỏ phải xuất trình bản gốc giấy uỷ quyền, giấy phép lưu hành và phiếu kiểm nghiệm sản phẩm

Hiệp định thương mại tự do Việt Nam - EU (EVFTA) có hiệu lực từ tháng 8/2020 mở ra nhiều cơ hội trong quan hệ đối tác toàn diện giữa hai bên. Tác động của EVFTA đến ngành dược phẩm đã có những kết quả dần rõ nét, đặc biệt là đối với các doanh nghiệp Châu Âu.

Việc duy trì sản xuất và giao hàng đúng hạn, giữ đúng cam kết với khách hàng là nỗ lực đáng ghi nhận, thể hiện uy tín, nội lực và sức cạnh tranh cao của Tiến Tuấn.

Theo Đại sứ quán Việt Nam tại Ấn Độ, đây là gợi ý được các ông lớn trong ngành dược phẩm Ấn Độ đưa ra trong buổi họp xúc tiến thương mại đầu tư do Đại sứ Việt Nam tại Ấn Độ - ông Phạm Sanh Châu chủ trì.

Bằng sự đồng lòng của tập thể công ty Tiến Tuấn và những chỉ đạo kịp thời của ban lãnh đạo, lô hàng đã được xuất đi thành công đến tay khách hàng tại thị trường châu Á.

Nhằm cung cấp cho quý bạn đọc và quý khách hàng những tin tức mới nhất về ngành công nghiệp dược phẩm Việt Nam và xu hướng sản xuất dược phẩm trên thế giới, cũng như cập nhật các tính năng mới, hiện đại về công nghệ sản xuất dược phẩm toàn cầu, chúng tôi sẽ đều đặn gửi đến bạn đọc các bản tin tổng hợp định kỳ mỗi tháng.

Thuật ngữ 'ngăn chặn' và 'cách ly' có ý nghĩa gì trong ngành dược phẩm? Tại sao các dây chuyền ung thư đều phải áp dụng hệ thống này?
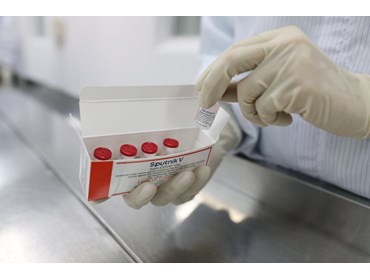
Lô vaccine Sputnik V thử nghiệm này mang lại hi vọng cho công cuộc tiêm chủng cộng đồng của Việt Nam.
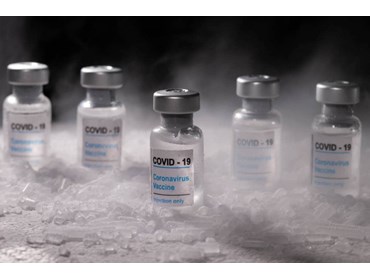
Trước năm 2020, khái niệm tủ đông lạnh âm sâu (ULT - Utra Low Temperature Freezers) được rất ít người biết đến, ngoài trừ giới y học và các ngành công nghiệp liên quan. Nhưng khi Pfizer thông báo vắc xin của họ yêu cầu bảo quản ở nhiệt độ -70 ° C, một thế giới đang quay cuồng tìm cách chống đại dịch đã dành sự quan tâm lớn đến khái niệm bảo quản “lạnh âm sâu”.

Nước rửa tay được xếp vào danh mục sản phẩm thuốc không kê đơn (OTC). Các triệu chứng đau đầu, buồn nôn và chóng mặt có thể xảy ra sau khi thoa nước rửa tay chứa cồn lên da. Những triệu chứng này có thể xảy ra do hít phải hơi từ nước rửa tay, có thể do tiếp xúc trong không gian kín hoặc những nơi không khí lưu thông kém… Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) vừa đưa ra cảnh báo về vấn đề rửa khuẩn tay trong mùa dịch bệnh.

Nhằm cập nhật cho bạn đọc những tin tức mới nhất về tình hình ngành dược phẩm hiện tại của Việt Nam và xu hướng sản xuất dược phẩm của thế giới, cũng như cập nhật các tính năng mới, hiện đại về công nghệ sản xuất dược phẩm toàn cầu, chúng tôi sẽ đều đặn gửi đến bạn đọc các bản tin ngắn hàng tháng.

Theo ước tính của WHO, gần 40 tỷ đô la bị mất mỗi năm cho các sản phẩm thuốc giả mạo. Một trong những biện pháp mà ngành dược thực hiện để vượt qua thách thức này là in số tuần tự hóa dược phẩm để bảo vệ người tiêu dùng; từ đó làm cho việc sản xuất hàng giả trở nên khó khăn hơn.

Bao viên dần trở thành công nghệ không thể thiếu trong ngành dược phẩm. Trong hơn 25 năm qua, lớp phủ viên đã trải qua một số thay đổi cơ bản. Nhiều cải tiến công nghệ bao đã được tiến hành để nâng cao chất lượng và quy trình sản xuất thuốc.
Có nhận định cho rằng công nghiệp dược truyền thống khá bảo thủ và vì vậy người ta có thể đưa ra vô số lý do từ quy chế cho đến nguồn lực tài chính để biện minh cho việc chậm trễ trong tiếp thu các công nghệ mới. Tuy nhiên, chắc chắn chúng ta sẽ chứng kiến những thay đổi mạnh mẽ và đầy sáng tạo trong công nghiệp dược phẩm trong những năm trước mắt khi Công nghiệp 4.0 đang trở thành một cuộc cách mạng công nghệ trên toàn cầu.
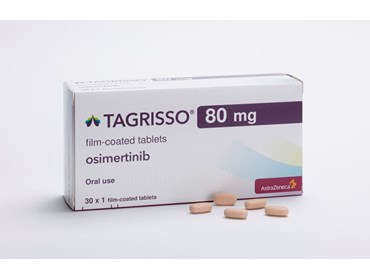
Ủy ban Châu Âu đã phê duyệt thuốc điều trị ung thư phổi như một phương pháp điều trị bổ sung cho người lớn được chẩn đoán đủ sớm để phẫu thuật cắt bỏ khối u và những người có đột biến gen EGFR
Công ty dược phẩm Việt Nam đang dần bị lép vế trước các đối thủ nước ngoài. Với hàng loạt các chính sách nới lỏng được đưa ra, thị trường dược phẩm Việt Nam là miếng bánh béo bở cho các công ty dược nước ngoài nhảy vào.
Với việc sản xuất bị tạm dừng và hàng triệu liều vắc-xin COVID-19 trong tình trạng lấp lửng, Johnson & Johnson đã hối hả đưa tàu đến ngay cơ sở sản xuất Baltimore đang gặp khó khăn của CDMO Emergent BioSolutions. Bây giờ, có vẻ như sự cứu trợ đang ở trong tầm mắt.

 Ngành dược nhạy cảm với Covid nhưng đang dần hồi phục. Dịch Covid-19 là thách thức lớn đối với toàn dân, các ngành sản xuất đặc biệt là ngành dược trong trường hợp lây lan mạnh trong cộng đồng. Tuy nhiên, tại thời điểm hiện tại, mục tiêu chăm sóc sức khỏe đang là mục tiêu chính và là khoản chi tiêu thiết yếu đối với người dân. Nhu cầu dược phẩm sẽ chỉ tạm thời bị trì hoãn trong ngắn hạn và sẽ dần phục hồi trở lại.
Ngành dược nhạy cảm với Covid nhưng đang dần hồi phục. Dịch Covid-19 là thách thức lớn đối với toàn dân, các ngành sản xuất đặc biệt là ngành dược trong trường hợp lây lan mạnh trong cộng đồng. Tuy nhiên, tại thời điểm hiện tại, mục tiêu chăm sóc sức khỏe đang là mục tiêu chính và là khoản chi tiêu thiết yếu đối với người dân. Nhu cầu dược phẩm sẽ chỉ tạm thời bị trì hoãn trong ngắn hạn và sẽ dần phục hồi trở lại.

(Theo Vietnamreport) Top 10 Công ty Dược uy tín được xây dựng dựa trên nguyên tắc khoa học và khách quan. Các công ty được đánh giá, xếp hạng dựa trên 3 tiêu chí chính: (1) Năng lực tài chính thể hiện trên báo cáo tài chính năm gần nhất; (2) Uy tín truyền thông được đánh giá bằng phương pháp Media Coding - mã hóa các bài viết về công ty trên các kênh truyền thông có ảnh hưởng; (3) Khảo sát các đối tượng liên quan được thực hiện trong tháng 10 và 11 năm 2020.

Đại dịch COVID-19 diễn ra vào những ngày cuối năm 2019 và chính thức bùng phát vào đầu năm 2020 kéo theo nhiều hệ lụy phức tạp, ảnh hưởng trực tiếp đến sức khỏe cộng đồng và kinh tế thế giới.
Tưởng chừng như ngành dược phẩm sẽ là ngành phát triển chính tại đại dịch Covid nhưng hoàn toàn ngược lại, ngành Dược Phẩm cũng như những ngành khác đã chịu nhiều thiệt hại do Covid mang tới.

AstraZeneca đã công bố kết quả thử nghiệm tại Mỹ với kết quả cuối cùng được đưa ra: trên 76% các tình nguyện viên được tiêm vaccine đạt miễn dịch tốt với Covid-19.


Hội thảo về chủ đề “Làm thế nào để xây dựng nhà máy dược phẩm đạt GMP-EU” đã được Tiến Tuấn tổ chức thành công vào ngày 18/08/2017 tại Phòng họp số 2 – Trung tâm triển lãm SECC, Nguyễn Văn Linh, Quận 7, TPHCM và cho thấy sự quan tâm đặc biệt của rất nhiều doanh nghiệp dược phẩm trong nước.

Nhằm giúp các Doanh nghiệp Việt Nam nắm bắt thông tin, tìm hiểu về các công nghệ bào chế tiên tiến nhất hiện nay trên thế giới. Công ty TNHH Chế tạo máy dược phẩm Tiến Tuấn kính gửi đến Quý Công ty thông tin về hội thảo "Telstar – Hệ thống cô lập" và "Natoli và giải pháp trọn vẹn cho công nghệ dập viên" được tổ chức tại trung tâm triển lãm Quốc tế Hà Nội – 91 Trần Hưng Đạo, Quận Hoàn Kiếm, TP Hà Nội.












